पानी में कठोरता का निर्धारण विभिन्न औद्योगिक और घरेलू अनुप्रयोगों के लिए एक महत्वपूर्ण पैरामीटर है। कठोरता मुख्य रूप से द्विसंयोजक धनायनों, मुख्य रूप से कैल्शियम (Ca2+) और मैग्नीशियम (Mg2+) की उपस्थिति के कारण होती है। एथिलीन डायमाइन टेट्रा एसिटिक एसिड (ईडीटीए) अनुमापन विधि को इसकी उच्च परिशुद्धता और विश्वसनीयता के कारण कठोरता को मापने के लिए व्यापक रूप से नियोजित किया जाता है।
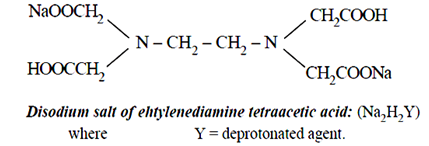
चूँकि शुद्ध EDTA पानी में अघुलनशील है, EDTA के डाई सोडियम लवण का उपयोग किया जाता है जो 2Na+ उत्सर्जित करता है और आयनित हो जाता है। इसे H2Y-2 के रूप में दर्शाया गया है।
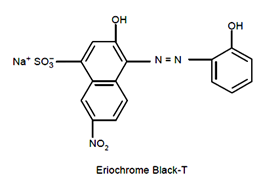
उपयोग किया गया संकेतक एक जटिल कार्बनिक यौगिक (सोडियम – 1 – (1-हाइड्रॉक्सी 2-नेफ्थिलाज़ो) -6-नाइट्रो-2-नेफ्थोल-4-सटफ़ोनेट) है, जिसे आमतौर पर एरियोक्रोम ब्लैक टी (ईबीटी) के रूप में जाना जाता है। इसमें दो आयनीकरण योग्य फेनोलिक हाइड्रोजन परमाणु हैं और सरलता के लिए इसे Na+H2In–के रूप में दर्शाया गया है:
कठोरता निर्धारण के लिए EDTA अनुमापन का सिद्धांत: EDTA एक बहुमुखी चेलेटिंग एजेंट है जो धातु आयनों के साथ स्थिर परिसरों का निर्माण करता है। पानी की कठोरता निर्धारण के संदर्भ में, प्रतिक्रिया में EDTA के साथ धातु आयनों (Ca2+ और Mg2+) का संयोजन शामिल होता है। कैल्शियम आयनों के साथ प्रतिक्रिया के लिए संतुलित रासायनिक समीकरण है:

प्रक्रिया: 1. नमूना संग्रह: अन्य धातु आयनों के हस्तक्षेप को रोकने के लिए पानी का नमूना एकत्र किया जाता है और उसे अम्लीकृत किया जाता है। 2. जटिल गठन: ज्ञात पीएच (आमतौर पर लगभग 10) के साथ एक बफर समाधान नमूने में जोड़ा जाता है। यह पीएच को उस स्तर पर बनाए रखता है जहां धातु-ईडीटीए जटिल गठन इष्टतम होता है। बफर अन्य धातु आयनों के हस्तक्षेप को भी रोकता है। 3. अनुमापन: अंतिम बिंदु तक पहुंचने तक एक मानकीकृत EDTA समाधान धीरे-धीरे नमूने में जोड़ा जाता है। समापन बिंदु को रंग परिवर्तन द्वारा चिह्नित किया जाता है, आमतौर पर वाइन-लाल से नीले रंग में, एरीओक्रोम ब्लैक टी या कैलमैगाइट जैसे धातु संकेतक के अतिरिक्त द्वारा सुविधा प्रदान की जाती है। 4.गणना: धातु आयनों को टाइट्रेट करने के लिए आवश्यक EDTA की मात्रा का उपयोग कठोरता की गणना के लिए किया जाता है। धातु आयनों की सांद्रता प्रतिक्रिया की स्टोइकोमेट्री और उपयोग किए गए EDTA समाधान की मात्रा का उपयोग करके निर्धारित की जा सकती है।

शामिल रासायनिक प्रतिक्रियाएँ:


यहां, H2Y-2 EDTA अणु का प्रतिनिधित्व करता है। इसी तरह की प्रतिक्रियाएँ मैग्नीशियम आयनों के साथ होती हैं। इन प्रतिक्रियाओं की स्टोइकोमेट्री 1:1 है, जिसका अर्थ है कि धातु आयन का एक मोल EDTA के एक मोल के साथ प्रतिक्रिया करता है। ये प्रतिक्रियाएं धातु-ईडीटीए परिसरों के निर्माण को प्रदर्शित करती हैं। अनुमापन के दौरान रंग परिवर्तन ईडीटीए के साथ धातु आयनों के उनके परिसरों से मुक्त होने के कारण होता है, जिसके परिणामस्वरूप संकेतक का रंग बदल जाता है।
EDTA अनुमापन के लाभ:
1. चयनात्मकता: ईडीटीए में कैल्शियम और मैग्नीशियम आयनों के लिए उच्च चयनात्मकता है, जो अन्य आयनों के हस्तक्षेप को कम करती है।
2. संवेदनशीलता: यह विधि उच्च परिशुद्धता के साथ धातु आयनों की कम सांद्रता का पता लगा सकती है।
3. बहुमुखी प्रतिभा: ईडीटीए अनुमापन विधि को कैल्शियम और मैग्नीशियम दोनों के निर्धारण के लिए अनुकूलित किया जा सकता है, जो कुल कठोरता प्रदान करता है।
निष्कर्षतः, EDTA अनुमापन विधि द्वारा पानी की कठोरता का निर्धारण एक विश्वसनीय और व्यापक रूप से स्वीकृत तकनीक है। धातु आयनों और ईडीटीए के बीच जटिल प्रतिक्रियाएं, उपयुक्त संकेतकों के उपयोग के साथ मिलकर, पानी के नमूनों में कठोरता की सटीक मात्रा निर्धारित करने में सक्षम बनाती हैं, जो विभिन्न औद्योगिक और घरेलू उद्देश्यों के लिए महत्वपूर्ण है।
